Các Định Luật Vật Lý Về Chất Khí
Chất khí, một trong ba trạng thái vật chất phổ biến, đóng vai trò quan trọng trong cuộc sống hàng ngày cũng như trong nhiều lĩnh vực khoa học kỹ thuật. Để hiểu rõ hơn về tính chất và ứng dụng của chất khí, chúng ta cần tìm hiểu về các định luật vật lý về chất khí. Những định luật này mô tả mối quan hệ giữa các đại lượng vật lý như áp suất, thể tích, nhiệt độ và số mol của một lượng khí xác định.
 Định luật Boyle-Mariotte
Định luật Boyle-Mariotte
Định luật Boyle-Mariotte
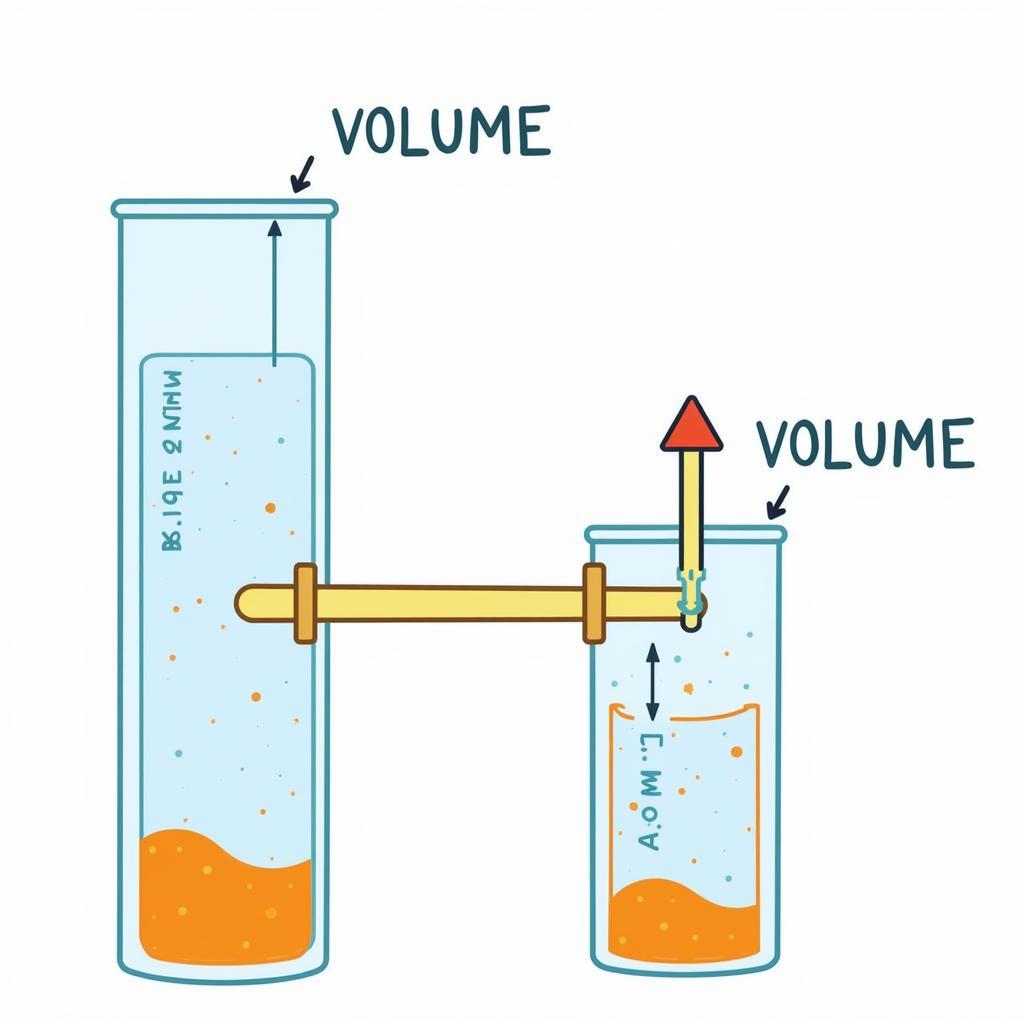
Định luật Boyle-Mariotte, được phát hiện bởi Robert Boyle và Edme Mariotte, mô tả mối quan hệ nghịch biến giữa áp suất và thể tích của một lượng khí xác định ở nhiệt độ không đổi.
Công thức: P₁V₁ = P₂V₂
Trong đó:
- P₁: Áp suất ban đầu của khí
- V₁: Thể tích ban đầu của khí
- P₂: Áp suất sau khi thay đổi
- V₂: Thể tích sau khi thay đổi
Ví dụ, khi ta bơm xe đạp, ta đang giảm thể tích của khí bên trong lốp xe, dẫn đến áp suất khí bên trong tăng lên.
Định luật Charles
Định luật Charles, được phát hiện bởi Jacques Alexandre Charles, mô tả mối quan hệ tỉ lệ thuận giữa thể tích và nhiệt độ tuyệt đối của một lượng khí xác định ở áp suất không đổi.
Công thức: V₁/T₁ = V₂/T₂
Trong đó:
- V₁: Thể tích ban đầu của khí
- T₁: Nhiệt độ tuyệt đối ban đầu của khí (đơn vị Kelvin)
- V₂: Thể tích sau khi thay đổi
- T₂: Nhiệt độ tuyệt đối sau khi thay đổi (đơn vị Kelvin)
Ví dụ, khi ta đun nóng một quả bóng bay, thể tích của quả bóng sẽ tăng lên do nhiệt độ của khí bên trong tăng.
Định luật Gay-Lussac
Định luật Gay-Lussac, được phát hiện bởi Joseph Louis Gay-Lussac, mô tả mối quan hệ tỉ lệ thuận giữa áp suất và nhiệt độ tuyệt đối của một lượng khí xác định ở thể tích không đổi.
Công thức: P₁/T₁ = P₂/T₂
Trong đó:
- P₁: Áp suất ban đầu của khí
- T₁: Nhiệt độ tuyệt đối ban đầu của khí (đơn vị Kelvin)
- P₂: Áp suất sau khi thay đổi
- T₂: Nhiệt độ tuyệt đối sau khi thay đổi (đơn vị Kelvin)
Ví dụ, khi ta để quên một bình xịt côn trùng trong cốp xe hơi nóng, áp suất khí bên trong bình sẽ tăng lên do nhiệt độ tăng, có thể dẫn đến nổ bình.
Phương trình trạng thái khí lý tưởng
Phương trình trạng thái khí lý tưởng kết hợp ba định luật trên, mô tả mối quan hệ giữa áp suất, thể tích, nhiệt độ và số mol của một lượng khí lý tưởng.
Công thức: PV = nRT
Trong đó:
- P: Áp suất của khí
- V: Thể tích của khí
- n: Số mol của khí
- R: Hằng số khí lý tưởng (R = 8.314 J/(mol·K))
- T: Nhiệt độ tuyệt đối của khí (đơn vị Kelvin)
Phương trình này cho phép ta tính toán một trong các đại lượng P, V, n, T khi biết ba đại lượng còn lại.
 Ứng dụng của định luật khí
Ứng dụng của định luật khí
Ứng dụng của các định luật vật lý về chất khí
Các định luật vật lý về chất khí có ứng dụng rộng rãi trong đời sống và khoa học kỹ thuật, ví dụ như:
- Trong kỹ thuật ô tô: Thiết kế động cơ đốt trong, hệ thống phanh khí nén, túi khí,…
- Trong y tế: Sử dụng khí nén trong máy thở, máy gây mê,…
- Trong công nghiệp thực phẩm: Bảo quản thực phẩm bằng khí nitơ, sản xuất đồ uống có ga,…
- Trong ngành hàng không: Điều khiển độ cao của máy bay, điều hòa áp suất trong khoang hành khách,…
Theo Luật sư Nguyễn Văn A, chuyên gia về luật khoa học công nghệ: “Việc hiểu rõ và áp dụng đúng đắn các định luật vật lý về chất khí đóng vai trò quan trọng trong việc đảm bảo an toàn và hiệu quả cho nhiều hoạt động sản xuất và đời sống.”
Kết luận
Các định luật vật lý về chất khí là nền tảng quan trọng để hiểu về tính chất và ứng dụng của chất khí. Nắm vững các định luật này giúp chúng ta giải thích nhiều hiện tượng tự nhiên, ứng dụng vào đời sống và phát triển khoa học công nghệ.
Câu hỏi thường gặp
1. Khí lý tưởng là gì?
Khí lý tưởng là mô hình lý tưởng hóa của khí thực, trong đó các phân tử khí được coi là các chất điểm không có thể tích và không tương tác với nhau ngoài va chạm đàn hồi.
2. Tại sao phải sử dụng nhiệt độ tuyệt đối trong các công thức?
Nhiệt độ tuyệt đối (đơn vị Kelvin) phản ánh động năng trung bình của các phân tử khí, trong khi nhiệt độ Celsius hay Fahrenheit không.
3. Các định luật vật lý về chất khí có áp dụng được cho chất lỏng và chất rắn không?
Không. Các định luật này chỉ áp dụng cho chất khí, bởi vì chất lỏng và chất rắn có thể tích và lực liên kết phân tử khác biệt.
Bạn cần hỗ trợ?
Nếu bạn có bất kỳ câu hỏi hoặc cần hỗ trợ về luật trò chơi điện tử, hãy liên hệ với chúng tôi:
- Số Điện Thoại: 0903883922
- Email: [email protected]
- Địa chỉ: Đoàn Thị Điểm, An Lộc, Bình Long, Bình Phước, Việt Nam.
Chúng tôi có đội ngũ chăm sóc khách hàng 24/7.